¿Cómo nos ayuda la tabla periódica a predecir patrones y tendencias en las propiedades de los elementos? 7 h
DEMOSTRACIÓN: Alcalinos en agua
La tabla periódica de los elementos clasifica a los mismos por orden creciente de número atómico, haciendo coincidir verticalmente a sustancias con similares propiedades químicas, lo que refleja a la postre una coincidencia de las configuraciones electrónicas de las mismas, como se ha indicado en la presentación anterior, y de hecho, es posible escribir la configuración electrónica de cualquier elemento, conociendo su posición en la tabla.
Las filas de la tabla se denominan periodos; el número del periodo indica el nivel energético más externo ocupado por electrones, es decir, la capa de valencia. A lo largo de los periodos hay una serie de propiedades que evolucionan de forma similar al compararlos entre sí.
Las columnas se llaman grupos; los elementos de un mismo grupo tienen el mismo número de electrones de valencia y consecuentemente, la misma configuración electrónica en la capa de valencia, lo que determina propiedades químicas muy similares entre sí.
Algunos de los grupos tienen nombres característicos: grupo 1, alcalinos; grupo 2, alcalinotérreos; grupos 3 a 12, metales de transición; grupo 13, térreos; grupo 16, anfígenos; grupo 17, halógenos; y grupo 18 gases nobles. Las dos series de 14 elementos que se suelen situar por comodidad fuera de la tabla se denominan lantánidos (periodo 6) y actínidos (periodo 7).
Las propiedades periódicas clásicas son cuatro:
- radio atómico, definido como la mitad de la distancia entre los centros de dos átomos vecinos iguales
- potencial de ionización, energía necesaria para arrancarle un electrón al átomo en estado gaseoso
- afinidad electrónica, energía desprendida cuando un átomo en fase gaseosa acepta un electrón transformándose en un anión
- electronegatividad, tendencia de un átomo a atraer hacia sí los electrones compartidos en un enlace
En este ENLACE se puede descargar un fichero con los datos y gráficos de las cuatro propiedades periódicas clásicas.
El radio atómico de un elemento viene determinado por el equilibrio entre dos factores:
- El apantallamiento del núcleo que hacen los electrones de las capas internas, que contribuye a que el tamaño crezca: cuanto más apantallado esté el núcleo, menor será la carga nuclear efectiva, y por lo tanto la atracción que sienten los electrones externos, que es lo que determina el tamaño del átomo
- La carga nuclear, que contribuye a que el tamaño disminuya: cuanto mayor la carga, mayor la atracción por los electrones externos y menor el tamaño.
A lo largo de un periodo, mientras se añaden electrones a la capa de valencia, el apantallamiento se mantiene constante, y lo que predomina es el efecto del aumento de la carga nuclear, por lo que el tamaño disminuye. Sin embargo, al bajar en un grupo, los electrones que median entre la capa de valencia y el núcleo apantallan muy bien al núcleo, por lo que el tamaño aumenta, a lo que se añade que los electrones se sitúan en un nuevo nivel.
Cabe en este punto hablar de los radios iónicos, en los que se pueden establecer algunas reglas sencillas:
- Los cationes siempre son más pequeños que los aniones (hay más protones para menos electrones)
- Entre los cationes, cuanto mayor sea la carga, más pequeño es el catión (por la misma razón anterior)
- Entre los aniones, cuanto mayor sea la carga, más grande será el anión (hay más electrones para menos protones)
En definitiva, el tamaño de los iones depende de la ratio electrones/protones: cuanto mayor sea (aniones), más grande es el ion y a la inversa.
La variación del potencial de ionización se puede explicar aludiendo al tamaño del átomo que hemos visto antes: cuanto más lejos esté el electrón (por un mayor apantallamiento del núcleo), menos energía hará falta para arrancárselo al átomo, y a la inversa. Por eso, la variación del potencial de ionización es la inversa a la del radio atómico. Los dientes de sierra que muestra la gráfica son consecuencia de que las configuraciones de capa llena o semillena son especialmente estables, y por ello, cuesta más energía romperlas, y menos alcanzarlas.
Otro tanto cabe decir de la afinidad electrónica, que puede verse como el potencial de ionización del anión correspondiente, cambiado de signo, y que por lo tanto, cabe esperar que se comporte igual que el potencial de ionización, y por los mismos motivos.
Finalmente, la electronegatividad, que también varía como el potencial de ionización y la afinidad electrónica. Si pensamos en qué es la electronegatividad, es fácil darse cuenta de que mide a la vez esas dos propiedades, y por ello no es sorprendente que varíe como ellas; un elemento con bajo potencial de ionización y baja afinidad electrónica tendrá muy poca tendencia a atraer hacia sí los electrones compartidos, y por lo tanto tendrá baja electronegatividad, y viceversa.
Los alcalinos reaccionan con agua, produciendo el hidróxido correspondiente e hidrógeno, que se libera e incluso puede llegar a entrar en ignición, debido a la energía que se libera en la reacción (es exotérmica):
M + H2O = M(OH) + ½ H2
Respecto a los halógenos, el poder oxidante decrece desde el flúor al yodo, por lo que el flúor es capaz de oxidar a los iones cloruro, bromuro y yoduro; el cloro al bromuro y el yoduro; y el bromo sólo al yoduro.
F2 > Cl2 > Br2 > I2
¬¾¾¾¾¾¾¾
PODER OXIDANTE
En esta WEB podéis explorar la periodicidad a lo largo del tercer periodo, específicamente el carácter ácido-base de los óxidos de los elementos del tercer periodo.
Óxidos básicos:
Óxidos básicos:
Na2O + H2O ¾® 2 NaOH
MgO + H2O ¾® Mg(OH)2
Óxido anfótero:
Al2O3 + 2 NaOH + 3 H2O ¾® 2 NaAl(OH)4
Al2O3 + 6 HCl ¾® 2 AlCl3 + 3 H2O
Óxidos ácidos:
SiO2 + 2 NaOH ¾® Na2SiO3 + H2O
CO2 + H2O ¾® H2CO3
SO3 + H2O ¾® H2SO4
SO2 + H2O ¾® H2SO3
P4O10 + 6 H2O ¾® 4 H3PO4
Cl2O5 + H2O ¾® 2 HClO3
Cl2O5 + H2O ¾® 2 HClO3
Puede verse que, conforme avanzamos por el periodo, el carácter básico se transforma gradualmente en ácido.
El estado de oxidación es la carga que tendría un elemento en un compuesto o especie química, si todos los enlaces fuesen iónicos. Para distinguirlo de la carga, se escribe el signo antes y el número después.
Para asignar estados de oxidación a los elementos de una especie, se siguen una serie de reglas:
- El número de oxidación de los elementos en estado puro es cero, p. ej.: Fe, P4 o N2.
- En los iones simples (un solo tipo de átomo), el número de oxidación coincide con la carga dividida por el número de átomos existentes, p.ej.: en el anión sulfuro (S2-), el estado de oxidación del azufre es –2, y en el peróxido (O22-), el del oxígeno es –1.
- El estado de oxidación del H es +1 salvo en los hidruros metálicos, que es –1.
- El estado de oxidación del O es –2 salvo en los peróxidos que vale –1.
- En moléculas neutras o iones complejos, la suma de todos los estados de oxidación de los elementos que la forman ha de ser igual a la carga (cero, si es una molécula neutra). Por ejemplo, en el ácido tiosulfúrico (H2S2O3), el H tiene estado de oxidación +1, y el O, -2; para el azufre: 2·(+1)+3·(-2)+2·n(S) = 0 por lo tanto 2-6+2·n(S) = 0 y n(S) = +2. O en el ión nitrosilo NO+, el O tiene –2, y entonces, el N ha de tener +3, para que la suma salga +1.
- Si la molécula es orgánica, se opera exactamente igual, asignando estados de oxidación a la fórmula molecular no desarrollada, por ejemplo, en el etanol (CH3-CH2OH = C2H6O), n(O)=-2, n(H)=+1 y n(C)=-2.
El siguiente gráfico muestra las energías de ionización sucesivas del átomo de silicio (1s2 2s2p6 3s2p2). Nótese que la escala del eje Y es logarítmica.
Como puede observarse, el gráfico muestra algunos saltos bruscos al pasar de cuarto al quinto potencial de ionizaicón y luego del duodécimo al décimotercero. El cuarto potencial de ionización corresponde a eliminar el último electrón 3s, y el quinto corresponde a arrancar el primer electrón 2p, es decir, pasamos del nivel 3 al nivel 2, y el salto brusco demuestra la existencia de esos niveles difernciados y separados por una diferencia energética significativa. Mientras se están quitando electrones de un mismo nivel, el aumento del potencial de ionización es paulatino, pero al cambiar de nivel, se da un salto brusco. Lo mismo ocurre del número 12 al número 13, que corresponden a quitar el último electrón 2s y el primero 1s respectivamente.
Cuando existen electrones 3d se puede apreciar lo mismo, aunque un tanto atenuado:
Los elementos del bloque d son todos metales, y se suelen denominar metales de transición, aunque el último de cada periodo (Zn, Cd, Hg) se suele sacar de esta clasificación por no compartir muchas de las propiedades de los demás. El electrón diferenciador de estos elementos llena el orbital 3d, según las reglas conocidas, con dos excepciones: Cr y Cu, que se deben memorizar:
Los metales de transición tienen las siguientes propiedades:
- Altas densidades y puntos de fusión y ebullición
- Gran diversidad de estados de oxidación, debido a la escasa diferencia entre los potenciales de ionización sucesivos, como se ha visto en 3.1.7.
- Propiedades catalíticas: muchas reacciones son aceleradas por metales de transición o algún complejo de coordinación suyo debido a que sus electrones desapareados y los niveles vacios o semillenos les pemiten unirse reversiblemente a gran cantidad de sustancias. Algunos ejemplos son la hidrogenación de alquenos (Ni), la eliminación de gases en el escape de los coches (Pt, Rh) o el proceso Haber (Fe).
- Propiedades magnéticas en forma elemental y combinado, dado que tienen electrones desapareados, los elementos y sus compuestos suelen ser paramagnéticos, dándose casos de ferromagnetismo también (Fe y Co). El momento magnético depende del número de electrones desapareados, hecho que se puede emplear para dilucidar estructuras.
- Forman aleaciones, debido a que tienen tamaños similares y pueden intercambiarse entre sí dentro de la red metálica; algunas de estas aleaciones tienen propiedades notables: acero inoxidable, acero al cromo, latón, bronce, etc.
- Forman complejos de coordinación coloreados que se abordan en el siguiente punto.
Estos compuestos contienen un ión de un metal de transición unido mediante enlaces covalentes dativos o coordinados a otras moléculas o iones llamados ligandos. También se pueden denominar compuestos de coordinación.
Los ligandos pueden ser monodentados, si solo pueden formar un enlace dativo, o polidentados o quelatos, si pueden formar varios.
- Ligandos monodentados: haluros, el agua o el amoniaco
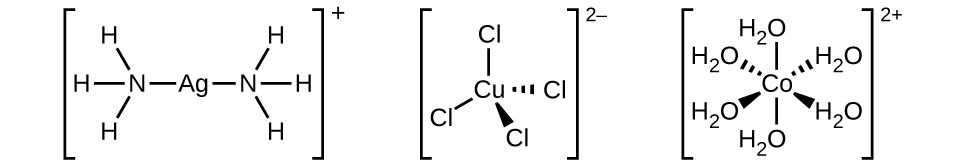
- Ligandos polidentados o quelatos: etilendiamina, oxalato, o AEDT

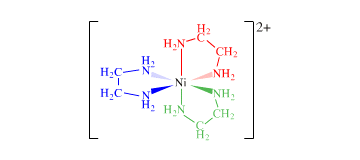

Muchos complejos con quelatos presentan isomería óptica:

El AEDT se emplea en la eliminación de metales pesados, en terapias de quelación, en tratamiento de aguas duras y como conservante alimentario.
Los complejos de coordinación presentan números de coordinación de 6 (octaédricos) o 4 (tetraédricos o plano cuadrados). Estas estructuras no se pueden deducir mediante la VSEPR, deben obtenerse del estudio de las estructuras por rayos X.
Estos complejos presentan una amplia variedad de colores, debido a que los ligandos inducen un desdoblamiento de los niveles d de modo que aparecen nuevas transiciones electrónicas entre estos subniveles desdoblados que caen en el rango del visible, de modo que el color del compuesto es el color complementario al de la radiación absorbida por la transición. La siguiente imagen corresponde a los complejos acuosos de los metales con la carga indicados:
La energía de la radiación absorbida es directamente proporcional a la frecuencia de la radiación o, lo que es lo mismo, inversamente proporcional a la longitud de onda de la misma.






























.png)
No hay comentarios:
Publicar un comentario